不銹鋼電化學拋光液一般含有硫酸、磷酸、鉻酐及少量的水,以及在電解過程中溶入的Fe3+、Cr3+、Ni2+、Mn2+等雜質。當采用標準堿液連續滴定時,這些金屬雜質的鹽類會水解,使分析結果偏高。因此,在滴定過程中要加入絡合劑掩蔽金屬雜質,以防止水解。絡合掩蔽劑采用六偏磷酸鈉或EDTA。
采用(yong)六偏磷(lin)(lin)酸鈉(na)時(shi)(shi),由于(yu)其(qi)水溶液pH=6,采用(yong)甲(jia)(jia)基紅和溴甲(jia)(jia)酚綠(lv)混合指(zhi)示劑在(zai)第一個等電(dian)點滴定時(shi)(shi)pH=5,所以六偏磷(lin)(lin)酸鈉(na)不(bu)消(xiao)耗堿(jian),用(yong)酚酞為(wei)指(zhi)示劑進行第二個等電(dian)點滴定時(shi)(shi)pH=9.5,六偏磷(lin)(lin)酸鈉(na)就會耗去相應量的(de)堿(jian),此(ci)堿(jian)量需(xu)在(zai)計算中扣除(chu)。其(qi)反(fan)應式如(ru)下。
第一(yi)個等電點時(pH=5):
H2SO4+2NaOH→Na2SO4+2H2O
H3PO4+NaOH→NaH2PO4+H2O
H2CrO4+NaOH→NaHCrO4+H2O
第二個等電點(dian)時(shi)(pH=9.5):
NaH2PO4+NaOH→Na2HPO4+H2O
NaHCrO4+NaOH→Na2CrO4+H2O
(NaPO3)6+6NaOH→6Na2HPO4
若是采用 EDTA,從絡合能(neng)力(li)看比(bi)六偏磷酸鈉(na)好(hao),但第(di)一個等電點(dian)時,0.05mol/L的EDTA溶液的pH約(yue)為4,離第(di)一個等電點(dian)較遠,需消(xiao)耗一定量的氫氧化鈉(na),到達第(di)二個等電點(dian)時進一步消(xiao)耗氫氧化鈉(na),需分別(bie)扣除。
扣(kou)除方法:取一個同本操作(zuo)中所(suo)加(jia)絡(luo)合掩(yan)蔽(bi)劑用(yong)量相(xiang)同的(de)絡(luo)合掩(yan)蔽(bi)劑,加(jia)水稀釋,進行空白(bai)實驗,(不加(jia)電化學(xue)拋光(guang)液),分別以甲(jia)基紅(hong)、溴甲(jia)酚(fen)綠指(zhi)示劑用(yong)氫(qing)(qing)氧(yang)化鈉(na)(na)標(biao)(biao)準液滴(di)定(ding)至(zhi)第一個等電點(dian),由紅(hong)變綠,記錄耗(hao)用(yong)的(de)氫(qing)(qing)氧(yang)化鈉(na)(na)毫(hao)升數(shu)(shu),以酚(fen)酞為指(zhi)示劑用(yong)氫(qing)(qing)氧(yang)化鈉(na)(na)標(biao)(biao)準液滴(di)至(zhi)第二個等電點(dian),由綠色變紫紅(hong)色,記錄耗(hao)用(yong)的(de)氫(qing)(qing)氧(yang)化鈉(na)(na)毫(hao)升數(shu)(shu),分別在計(ji)算中減去。
1. 試劑(ji)
①. 標準0.5mol氫氧化鈉(na)溶液。稱取20g氫氧化鈉(na)溶于蒸餾(liu)水中(zhong),用水在量(liang)瓶中(zhong)稀(xi)釋至1L.
標(biao)定(ding):稱取在120℃干(gan)燥2h后的(de)分析(xi)純苯二甲酸氫鉀(KHC8H4O4)4g(四位有效數字P)于250mL錐形杯(bei)中,加(jia)水(shui)100mL,溫熱(re)使其(qi)溶解,加(jia)入酚酞指示劑2滴,用配制好的(de)氫氧化鈉(na)溶液(ye)滴定(ding)至淡(dan)紅(hong)色為(wei)終點,記錄耗用的(de)氫氧化鈉(na)溶液(ye)為(wei)V(mL)。
計算:標準(zhun)氫氧化鈉(na)溶液的摩爾濃(nong)度(du)
M= P × 1000 / V × 204.2 (mol/L)
②. 0.1mol六偏(pian)磷酸的溶(rong)液。稱取120℃干(gan)燥2h后的分析純六偏(pian)磷酸鈉61.20g,溶(rong)于(yu)蒸餾水中,用水在容量瓶(ping)中稀釋至1L。不需標(biao)定(ding)。
③. 0.05mol EDTA標準溶液。②和③中兩者擇其一,稱取分析純EDTA(乙二胺四乙酸二鈉,其分子式C10H14N2O8Na2·2H2O)20g,溶解于熱蒸餾水中,冷卻后,用水在容量瓶中稀釋至1L。
標定:稱(cheng)取分析純金屬(shu)鋅(xin)0.4g(準確稱(cheng)重至(zhi)(zhi)(zhi)四(si)位(wei)有效數字P),在250mL錐形瓶(ping)中(zhong)用(yong)1:1試劑鹽酸(suan)加(jia)熱溶(rong)(rong)(rong)解鋅(xin)至(zhi)(zhi)(zhi)完全(quan)形成氯(lv)化(hua)鋅(xin),冷卻,移入100mL容量瓶(ping)中(zhong),加(jia)水(shui)稀釋至(zhi)(zhi)(zhi)刻度(du),搖勻。用(yong)移液(ye)管吸取20mL于250mL錐形瓶(ping)中(zhong),加(jia)水(shui)50mL,以(yi)氨水(shui)調節至(zhi)(zhi)(zhi)微堿性,加(jia)入pH=10緩沖溶(rong)(rong)(rong)液(ye)(溶(rong)(rong)(rong)解54g氯(lv)化(hua)銨于水(shui)中(zhong),加(jia)入350mL濃氨水(shui),加(jia)水(shui)稀釋至(zhi)(zhi)(zhi)1L)10mL,鉻(ge)(ge)黑T指示劑(0.5g鉻(ge)(ge)黑T和氯(lv)化(hua)鈉50g研磨而成)少許,搖勻,以(yi)配好的0.05mol EDTA標準溶(rong)(rong)(rong)液(ye)滴定至(zhi)(zhi)(zhi)由紅變藍色為終點,記(ji)錄耗(hao)用(yong)的EDTA溶(rong)(rong)(rong)液(ye)V(mL).
計算:標準EDTA溶液(ye)濃度
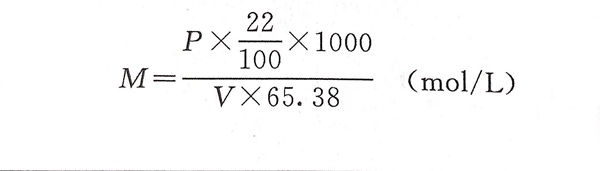
④. 甲基紅指示劑(pH 4.2~6.3).稱取(qu)甲基紅0.1g溶(rong)解于60mL乙(yi)醇中(zhong),溶(rong)解后加水(shui)稀(xi)釋至(zhi)100mL。
⑤. 溴甲酚綠指(zhi)示劑(pH 3.6~5.2).稱取溴甲酚綠0.1g溶解(jie)于2.88mL的0.05mol氫氧化鈉溶液中,加水稀釋至250mL。
⑥. 酚(fen)酞指示劑(pH 8.3~10.0).稱取1g酚(fen)酞溶解(jie)(jie)于80mL乙醇中,溶解(jie)(jie)后加水稀釋至100mL.
2. 分析(xi)方(fang)法
①. 用六偏磷酸鈉(na)作(zuo)掩蔽(bi)劑。
a. 吸取試液5mL于250mL容量瓶中,加水稀釋至刻(ke)度,搖勻。
b. 吸取此液10mL于300mL錐(zhui)形(xing)瓶中(相當于原液0.2mL),加水80mL。
c. 用移液(ye)管(guan)準確加(jia)人(ren)六偏磷酸鈉溶(rong)液(ye)20mL。
d. 加甲基(ji)紅(hong)4滴(di)、溴甲酚綠6滴(di)。
e. 以0.5mol氫(qing)氧化鈉(na)標準溶液(ye)滴(di)定(ding)至綠色為終點,記(ji)錄耗用量V1。
f. 加酚酞5滴(di)。
g. 以(yi)0.5mol氫氧(yang)化鈉標(biao)準溶液(ye)滴定至紅色(保持20s不退(tui)),記錄(lu)耗用量V2。
h. 另用移液(ye)管(guan)吸取(qu)0.1mol六偏磷酸鈉(na)溶液(ye)20mL于250mL錐形(xing)瓶中(zhong),加水(shui)80mL。
i. 加(jia)酚酞5滴。
j. 用0.5mol氫氧化鈉溶液滴定(ding)至紅色,記錄耗(hao)用量B(mL)。
計算:
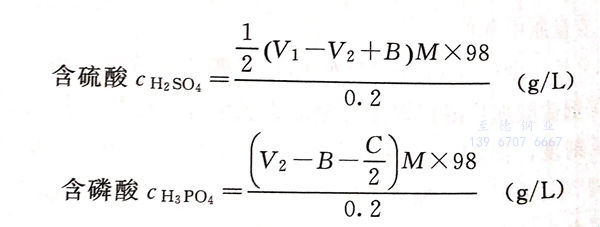
式中,M為標準氫氧化鈉溶液的摩爾濃度;C為中和所取試液中的CrO3相的標準氫氧化鈉溶液的容積,mL。
設n為所取試(shi)樣容積,mL;ck為三氧化鉻(ge)濃(nong)度,g/L;x為所取試(shi)樣中(zhong)含氧化鉻(ge)質量,g;
則(ze)有:
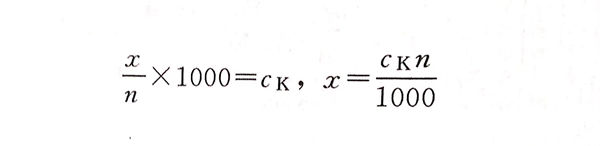

②. 用EDTA作掩蔽劑。
a. 吸取(qu)試液(ye)5mL于250mL容量瓶中(zhong),加(jia)水稀釋(shi)至刻度,搖勻。
b. 吸取此液10mL于300mL錐形瓶中(zhong)(相當于原液0.2mL),加水80mL。
c. 用移液管準(zhun)確加(jia)入0.05mol EDTA標準(zhun)溶液20mL。
d. 加甲基紅4滴、溴(xiu)甲酚(fen)綠6滴。
e. 用0.5mol氫氧化鈉標準溶液滴定至綠色為終點,記錄耗用量為V1。
f. 加酚酞5滴。
g. 用0.5mol氫氧化鈉標準溶液滴定至紅色(保持20s不褪色),記錄耗用量為V2。
h. 另用(yong)滴定管取0.05mol EDTA于250mL錐形(xing)瓶中,加水80mL。
i. 加甲基紅4滴,溴甲酚綠6滴。
j. 用(yong)0.05mol氫氧化鈉溶液滴定至綠色,記錄耗用(yong)量為(wei)A。
k. 加酚酞5滴。
l. 繼續用(yong)0.05mol氫氧化鈉溶液(ye)滴定(ding)至紅色(se),記錄耗用(yong)量為(wei)B。
計(ji)算:
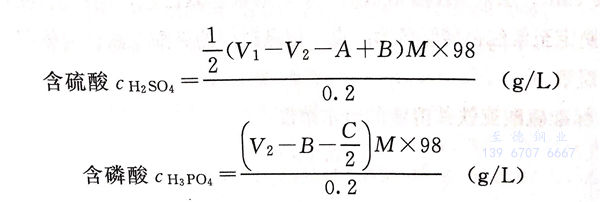
C 的(de)計算與①用六(liu)偏磷(lin)酸鈉掩蔽的(de)公式相同。



