1. 方法原理
在硫酸(suan)溶液中,六價鉻被亞(ya)鐵離(li)子還原為三價鉻:
2H2CrO4+6H2SO4+6FeSO4 = Cr2(SO4)3+3Fe2(SO4)3+8H2O
以苯基代(dai)鄰氨基苯甲酸(PA酸)為指示(shi)劑指示(shi)反應終點(dian)。
三價(jia)鉻在酸(suan)性溶液中,在硝酸(suan)銀催(cui)化(hua)下,以過硫酸(suan)銨氧化(hua)成六價(jia)銘,得到總鉻量。
Cr2(SO4)3+3(NH4)2S2O8+8H2O=-2H2CrO4+3(NH4)2SO4+6H2SO4
然后測定總鉻量消耗(hao)的(de)亞鐵(tie)量減(jian)去(qu)六(liu)價鉻消耗(hao)的(de)亞鐵(tie)量,即(ji)得三價鉻量。
硝(xiao)酸(suan)銀(yin)(yin)對(dui)氧(yang)化反應(ying)起催化作用(yong),銀(yin)(yin)離子和過(guo)(guo)硫(liu)酸(suan)銨生成(cheng)(cheng)過(guo)(guo)硫(liu)酸(suan)銀(yin)(yin),過(guo)(guo)硫(liu)酸(suan)銀(yin)(yin)能將三價(jia)鉻(ge)(ge)氧(yang)化成(cheng)(cheng)六(liu)價(jia)鉻(ge)(ge)。氧(yang)化反應(ying)完(wan)成(cheng)(cheng)后(hou),硝(xiao)酸(suan)銀(yin)(yin)仍恢(hui)復原來的(de)狀(zhuang)態。過(guo)(guo)量的(de)過(guo)(guo)硫(liu)酸(suan)銨對(dui)測定有干擾作用(yong),必須經煮沸后(hou)完(wan)全分解出氧(yang)氣。分解反應(ying)如下(xia):
2(NH4)2S2O8+2H2O = 2(NH4)2SO4+2H2SO4+O2↑
2. 試(shi)劑(ji)
①. 硫酸
1+1,即1體積分(fen)量的(de)硫酸加入1體積分(fen)量的(de)水(shui)中。
②. 苯基代鄰氨(an)基苯甲酸(PA酸)指(zhi)示劑
0.27g PA酸溶(rong)于5mL的5%碳酸鈉溶(rong)液中(zhong),以水稀釋(shi)至250mL.
③. 標準0.1mol硫酸亞鐵銨溶液
配制:稱取分析純硫酸亞鐵銨40g[FeSO4·(NH4)SO4·6H2O]溶于冷的5+95硫酸(5體積分量的硫酸溶于95體積分量的水中)500mL中,溶解完畢后以5+95硫酸稀釋至1L.亞鐵溶液在空氣中易氧化,應加入純鋁片若干,以還原被氧化的高鐵。應于使用前定期標定。鋁片的存在,有效維持亞鐵離子濃度的穩定(1個月左右)。同時投入少量NaHCO3,產生的CO2氣體隔絕空氣的氧化。
標(biao)定(ding)(ding):以重(zhong)鉻(ge)(ge)酸(suan)鉀標(biao)定(ding)(ding)。用移液管吸取標(biao)準0.1mol重(zhong)鉻(ge)(ge)酸(suan)鉀溶(rong)液(配(pei)(pei)制:取分析(xi)純重(zhong)鉻(ge)(ge)酸(suan)鉀于(yu)(yu)150℃干燥(zao)1h,在干燥(zao)器內冷(leng)卻,準確稱取29.421g,溶(rong)解于(yu)(yu)水,在量瓶中(zhong)稀釋至1L.不需(xu)標(biao)定(ding)(ding))10mL于(yu)(yu)250mL錐形瓶中(zhong),加(jia)水70mL及1+1 硫酸(suan)10mL,磷酸(suan)1mL.加(jia)入PA酸(suan)指示劑4滴,溶(rong)液呈紫紅色(se),用配(pei)(pei)制好(hao)的(de)0.1mol 硫酸(suan)亞(ya)鐵(tie)銨(an)溶(rong)液滴定(ding)(ding)至紫紅色(se)轉綠色(se)為終點,記錄耗用的(de)硫酸(suan)亞(ya)鐵(tie)銨(an)的(de)體(ti)積V(mL)。(終點前應逐(zhu)滴觀察。)
計算:標準硫(liu)酸亞鐵銨(an)溶液(ye)的摩爾濃度
M= 10×0.1×6 / V(mol/L)
④. 1%硝(xiao)(xiao)酸銀溶(rong)液。稱取1g重的硝(xiao)(xiao)酸銀溶(rong)解于100mL水中。或用(yong)0.1mol/L硝(xiao)(xiao)酸銀標準溶(rong)液。
⑤. 過硫酸(suan)銨。固體。
3. 分析方法
①. 吸取電解(jie)液各5mL于(yu)A、B兩(liang)個(ge)250mL錐(zhui)形(xing)瓶中,各加(jia)水50mL(A、B各用于(yu)測定(ding)鉻酐和三價鉻之用)。
②. 各加1+1硫(liu)酸(suan)10mL.
③. 于B瓶中加硝(xiao)酸銀10mL.
④. 于B瓶中加過硫酸銨2g,煮沸至冒大氣泡2min左右,冷卻。
⑤. 向A、B兩瓶中加PA酸5滴(di),搖勻。
⑥. 用(yong)標(biao)準(zhun)0.1mol硫酸亞(ya)鐵(tie)銨(an)溶(rong)液滴(di)定A、B兩瓶(ping)各(ge)至由紫(zi)紅色變(bian)綠色為終點(dian),記(ji)錄分(fen)析(xi)A、B各(ge)耗用(yong)標(biao)準(zhun)硫酸亞(ya)鐵(tie)銨(an)溶(rong)液各(ge)為V1和V2的(de)體(ti)積(mL)。V1為分(fen)析(xi)鉻酐時(shi)耗用(yong)硫酸亞(ya)鐵(tie)銨(an)溶(rong)液的(de)體(ti)積(mL),V2為分(fen)析(xi)總鉻酐時(shi)耗用(yong)硫酸亞(ya)鐵(tie)銨(an)溶(rong)液的(de)體(ti)積(mL).
4. 計算(suan)
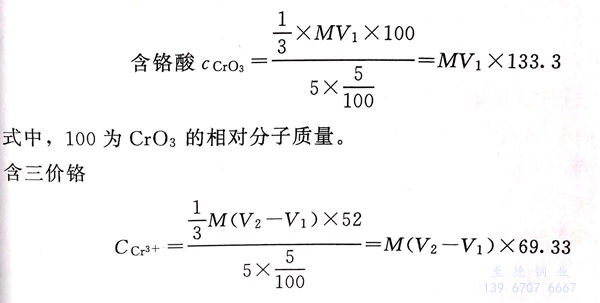
式中,52為Cr的(de)相對原子質量。
注:如果(guo)鉻(ge)酐或三價鉻(ge)含量過高(gao),可適當減(jian)少電解液所(suo)取體積。



